Tìm tìm phương trình hóa học đơn giản và dễ dàng và sớm nhất có thể tại h3qvn.com. Học tập Hóa không thể là nỗi lo lắng với phân mục Phương trình chất hóa học của chúng tôi
phản bội ứng hóa học là gì
Phản ứng hóa học là một quá trình dẫn đến đổi khác một tập hợp các chất này thành một tập hợp những chất khác. Theo cách cổ điển phản ứng hóa học bao gồm toàn cỗ các biến đổi chỉ tương quan đến vị trí của các electron phản bội ứng chất hóa học là một quy trình dẫn đến đổi khác một tập hợp những chất này thành một tập hợp các chất khác. Theo cách cổ điển phản ứng hóa học bao hàm toàn bộ các biến đổi chỉ tương quan đến vị trí của những electron
| (NH4)2CO3 | + | 2HCl | ⟶ | H2O | + | 2NH4Cl | + | CO2 | |
| rắn | lỏng | lỏng | rắn | khí | |||||
| không màu | khói trắng |
| 3Ag2SO4 | + | 2FeCl3 | ⟶ | 6AgCl | + | Fe2(SO4)3 | |
| rắn | dung dịch | kt | dung dịch | ||||
| trắng | vàng nâu | trắng | vàng nâu nhạt |
| Ag | + | 2HNO3 | ⟶ | AgNO3 | + | H2O | + | NO2 | |
| rắn | dd đậm đặc | rắn | lỏng | khí | |||||
| trắng bạc | không màu | trắng | không màu | nâu đỏ |
| Ag | + | 2HNO3 | ⟶ | AgNO3 | + | H2O | + | NO2 | |
| rắn | dd đậm đặc | rắn | lỏng | khí | |||||
| trắng bạc | không màu | trắng | không màu | nâu đỏ |
| Ag2O | + | H2O2 | ⟶ | 2Ag | + | H2O | + | O2 | |
| lỏng | rắn | lỏng | khí | ||||||
| vàng nhạt | không màu | trắng | không màu | không màu |
| Br2 | + | 5Cl2 | + | 6H2O | ⟶ | 10HCl | + | 2HBrO3 | |
| khí | khí | lỏng | lỏng | lỏng | |||||
| không màu | không màu | không màu | không màu | không màu |
| 3C | + | 2KNO3 | + | S | ⟶ | K2S | + | N2 | + | 3CO2 | |
| rắn | rắn | rắn | rắn | khí | khí | ||||||
| đen | đen | không màu | không màu |
| 3Br2 | + | C6H5NH2 | ⟶ | C6H2Br3NH2 | + | 3HBr | |
| dung dịch | lỏng | kt | dung dịch | ||||
| nâu đỏ | không màu | trắng | không màu |
| 3Br2 | + | C6H5NH2 | ⟶ | C6H2Br3NH2 | + | 3HBr | |
| dung dịch | lỏng | kt | dung dịch | ||||
| nâu đỏ | không màu | trắng | không màu |
| 3C2H4 | + | 4H2O | + | 2KMnO4 | ⟶ | 2KOH | + | 2MnO2 | + | 3C2H4(OH)2 | |
| khí | lỏng | rắn | dung dịch | kt | lỏng | ||||||
| không màu | không màu | tím | không màu | đen | không màu |
| Cl2 | + | H2S | ⟶ | 2HCl | + | S | |
| khí | khí | dung dịch | kt | ||||
| không màu | không màu,mùi sốc | không màu | đen |
| 6HCl | + | Cr2O3 | ⟶ | 3H2O | + | 2CrCl3 | |
| dung dịch | rắn | lỏng | rắn | ||||
| không màu | lục sẫm | không màu | tím đỏ |
| H2O | + | CH3COOC2H5 | ⟶ | C2H5OH | + | CH3COOH | |
| lỏng | lỏng | lỏng | dung dịch | ||||
| không màu | không màu | không màu |
| C2H5OH | + | H2NCH2COOH | ⟶ | H2O | + | H2NCH2COOC2H5 | |
| lỏng | lỏng | lỏng | rắn | ||||
| không màu | không màu | không màu |
| Ca(OH)2 | + | CO2 | ⟶ | CaCO3 | + | H2O | |
| dung dịch | khí | kt | lỏng | ||||
| không màu | không màu | trắng | không màu |
| NaOH | + | NH4NO3 | ⟶ | H2O | + | NaNO3 | + | NH3 | |
| dung dịch | rắn | lỏng | rắn | khí | |||||
| không màu | không màu | trắng | không màu,mùi khai |
| 3Cu | + | 4H2SO4 | + | 2NaNO3 | ⟶ | 4H2O | + | Na2SO4 | + | 2NO | + | 3CuSO4 | |
| rắn | dung dịch | rắn | lỏng | rắn | khí | ||||||||
| đỏ | không màu | trắng | không màu | trắng | không màu |
| C2H5OH | + | CH3COOH | ⇌ | H2O | + | CH3COOC2H5 | |
| lỏng | lỏng | lỏng | lỏng | ||||
| không màu | không màu | không màu |
| C2H5OH | + | HCOOH | ⟶ | H2O | + | HCOOC2H5 | |
| lỏng | dung dịch | lỏng | dd | ||||
| không màu | không màu | không màu |
| AgNO3 | + | H2O | + | 3NH3 | ⟶ | NH4NO3 | + | (Ag(NH3)2)OH | |
| rắn | lỏng | khí | rắn | rắn | |||||
| trắng | không màu | không màu |
| 4AgNO3 | + | 3CH3CHO | + | 5NH3 | ⟶ | 4Ag | + | 3NH4NO3 | + | 3CH3COONH4 | |
| rắn | dd | khí | kt | rắn | rắn | ||||||
| trắng | không màu | không màu,mùi khai | trắng | trắng | trắng |
| CH3CHO | + | 2Ag(NH3)2OH | ⟶ | 2Ag | + | H2O | + | 3NH3 | + | CH3COONH4 | |
| dung dịch | dung dịch | kt | khí | dung dịch | |||||||
| không màu | không màu |
| 2KMnO4 | + | 2KOH | ⟶ | H2O | + | O2 | + | 2K2MnO4 | |
| dung dịch | dung dịch | lỏng | khí | dung dịch | |||||
| tím | không màu | không màu | lục |
| NaOH | + | CH3-CCl3 | ⟶ | CH3COOH | + | H2O | + | NaCl | |
| dung dịch | khí | dung dịch | lỏng | rắn | |||||
| không màu | không màu | trắng |
Phương trình chất hóa học - đều điều bạn phải biết
Hóa học là một bộ môn thân thuộc với các bạn học sinh từ cấp cho Trung học cơ sở trở lên. Với Hóa học tập cũng là một trong những bộ môn “gây thù chuốc oán” các nhất với các bạn học sinh. Đây cũng chính là môn học sở hữu những tấm hình chế “có 1 - 0 - 2” bá đạo nhất.
Bạn đang xem: Tìm kiếm phương trình hóa học
Nội dung chính
- I. Tổng quan liêu phương trình hóa học 4. Cách cân đối phương trình hóa học II. Các công cụ buộc phải dùng khi tham gia học môn chất hóa học III. Những xem xét trong lịch trình Hóa họcI. Tổng quan tiền phương trình hóa học
1. Phương trình hóa học là gì?
Phương trình hóa học là phương trình trình diễn ngắn gọn phản ứng hóa học.
(Phản ứng hóa học là quá trình gây thay đổi từ một tập hợp hóa chất này thành một tập hợp hóa chất khác, phản ứng hóa học xảy ra khi tất cả những đk thích hợp).
Trong phương trình hóa học, những chất sẽ tiến hành biểu diễn dưới dạng kí hiệu hóa học của hóa học đó. Hóa học ở phía trái mũi tên là hóa học tham gia và chất bên cần mũi tên là chất sản phẩm.
Ví dụ: Hidro + Oxi -> Nước
(H_2 + O_2 ightarrow H_2O)
Chất tham gia:(H_2; O_2)
Chất sản phẩm:(H_2O)
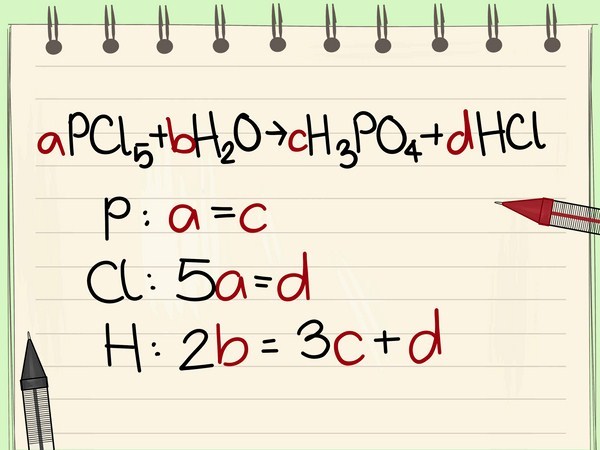
Cân bởi phương trình hóa học
2. Ý nghĩa phương trình hóa học
Biểu diễn ngắn gọn những phản ứng hóa học
Cho ta biết tỉ trọng về số nguyên tử, số phân tử giữa những chất cùng giữa những cặp chất trong phản nghịch ứng hóa học. Tỉ lệ này bởi tỉ lệ thông số giữa các chất vào phương trình hóa học.
3. Công việc lập phương trình hóa học
Để lập phương trình hóa học, chúng ta cần làm lần lượt 3 cách sau:
Bước 1: Viết sơ thiết bị phản ứng (gồm kí hiệu hóa học của những chất gia nhập và các chất sản phẩm)
Bước 2: cân đối số nguyên tử của mỗi nguyên tố, kiếm tìm số phù hợp đặt trước những công thức làm thế nào để cho số nguyên tử các nguyên tố ở chất tham gia với chất sản phẩm phải bằng nhau.
Bước 3: kết thúc phương trình hóa học.
4. Cách thăng bằng phương trình chất hóa học
Cân bằng phương trình hóa học là việc cân bởi về con số nguyên tố của những chất trong nhì vế của 1 phản ứng hóa học.
4.1. Phương pháp nguyên tử nguyên tốĐây là phương pháp đơn giản nhất.
Cân bằng theo phong cách này, ta đang viết những đơn hóa học khí bên dưới dạng nguyên tử riêng rẽ biệt.
Ví dụ: thăng bằng phương trình hóa học:(P_2 + O_5 ightarrow P_2O_5)
Để tạo thành thành 1 phân tử (P_2O_5), ta đề nghị 2 phân tử p. Và 5 phân tử O.
=> Ta được phương trình:
(2P + dfrac52 O_2 ightarrow P_2O_5)
Nhân các phân số với mẫu mã số chung nhỏ tuổi nhất (ở phương trình này là 2) ta sẽ được phương trình chất hóa học cuối cùng:
(P + 5O_2 ightarrow P_2O_5)
4.2. Phương thức hóa trị tác dụngHóa trị tính năng là số hóa trị của các nhóm nguyên tử giỏi nguyên tử của các nguyên tố tất cả trong bội phản ứng hóa học.
Các bước cân bằng với phương thức này:
Bước 1: xác minh hóa trị tác dụng
(BaCl_2 + Fe_2(SO_4)_3 ightarrow BaSO_4 + FeCl_3)
Hóa trị tác dụng lần lượt của phương trình trên từ trái qua cần là:
I - II - III - I - I - I - III - II
Bước 2: tìm bội số chung nhỏ tuổi nhất của các hóa trị tác dụng
Bội số chung nhỏ nhất của (I,II,III) là 6.
Bước 3: đem bội số chung bé dại nhất chia cho những hóa trị ta sẽ tiến hành hệ số sau:
6 : 1 = 6
6: 2 = 3
6: 3 =2
Bước 4: nắm vào phương trình phản bội ứng
4.3. Cách thức chẵn - lẻDựa vào nguyên tắc: sau khoản thời gian cân bằng, số nguyên tử của thành phần ở chất tham gia phải thông qua số nguyên tử của yếu tắc ở chất sản phẩm. Vậy cần nếu số nguyên tử của một nguyên tố ở một vế là số chẵn, thì nó cũng sẽ phải là số chẵn sinh sống vế còn lại. Yêu cầu nếu số nguyên tử của yếu tố còn lẻ, thì yêu cầu nhân đôi
Thí dụ: (FeS_2 + O_2 ightarrow Fe_2O_3 + SO_2)
Ở vế trái, số nguyên tử (O_2) là chẵn
Ở vế phải, số nguyên tử (O_2) trong (SO_2) là chẵn, tuy vậy số nguyên tử trong (Fe_2O_3) lại là lẻ. => nên nhân đôi. Sau đó, ta cân nặng bằng các hệ số còn lại
(2Fe_2O_3 ightarrow 4FeS_2 ightarrow 8SO_2 ightarrow 11O_2)
Phương trình được cân nặng bằng:
(4FeS_2 + 11O_2 ightarrow 2Fe_2O_3 + 8SO_2)
4.4. Cân bằng dựa vào nguyên tố phổ biến nhấtVới cách thức này, ta sẽ chọn lọc nguyên tố xuất hiện ở nhiều chất tốt nhất trong phản ứng.
Ví dụ: (Cu + HNO_3 ightarrow Cu(NO_3)_2 + NO + H_2O)
Nhận thấy, oxi là nguyên tố có mặt nhiều nhất trong phương trình làm phản ứng.
Vế phải bao gồm 8 oxi, vế phải gồm 3 oxi.
BSCNN của 3 và 8 là 24
=> Ghi 8 vào trước HNO3. Ta có:
(8HNO_3 ightarrow 4H_2O ightarrow 2NO)
Phương trình hóa học sau khi được cân nặng bằng:
(3Cu + 8HNO_3 ightarrow 3Cu(NO_3)_2 + 2NO + 4H_2O)
4.5. Cân đối theo phương thức đại sốDựa theo nguyên tắc: Số nguyên tử của những nguyên tử ở 2 vế phải bằng nhau.
Các cách làm:
Bước 1: Điền các hệ số a,b,c,d,e,... Vào trước những chất trong phản nghịch ứng.
Xem thêm: Top 12 Shop Bán Dụng Cụ Vẽ Online Ở Hà Nội Giá Rẻ Nhất 2021, Dụng Cụ Vẽ, Mỹ Thuật
Ví dụ: (aFeS_2 +bO_2 ightarrow cFe_2O_3 + dSO_2)
Bước 2: dùng định luật bảo toàn khối lượng để thăng bằng nguyên tố và tạo ra 1 phương trình đại số.
Fe: a = 2c
S: 2a = d
O: 2b = 3c + 2d.
Giải hệ phương trình có 3 phương trình trên.
Chọn c = 1 => a = 2, d = 4 và b =11/2.
Nhân các hệ số với 2, ta được phương trình cân nặng bằng:
(4FeS_2 + 11O_2 ightarrow 2Fe_2O_3 + 8SO_2)
II. Các công cụ phải dùng lúc học môn Hóa học
1. Bảng tuần trả nguyên tố hóa học (Nguyên tố hóa học)

Bảng tuần hoàn nguyên tố hóa học
Bảng tuần trả nguyên tố chất hóa học (gọi tắt là Bảng tuần hoàn) là một trong bảng gồm liệt kê lại những nguyên tố hóa học, dựa vào số hiệu nguyên tử (chính là số proton trong hạt nhân), thông số kỹ thuật e (electron) và các đặc thù hóa học của chúng. Các nguyên tố trong bảng được bố trí theo chiều tăng nhiều số hiệu nguyên tử.
Một bảng tiêu chuẩn gồm những nguyên tố hóa học được xếp thành 7 chiếc và 18 cột, 2 loại kép đơn nhất nằm dưới cùng bảng. Những hàng trong bảng sẽ được gọi là chu kì, còn cột sẽ được gọi là nhóm. Một số những nguyên tố sẽ sở hữu được những tên gọi đặc biệt: Halogen, khí hiếm.
Tất cả các phiên phiên bản của bảng tuần trả chỉ bao gồm các yếu tố hóa học, không bao hàm hỗn hợp, hợp chất,...
Bảng tuần trả nguyên tố hóa học không thiếu thốn và rõ rệt nhất.
2. Dãy chuyển động hóa học tập của kim loại
Dãy vận động hóa học tập của kim loại là dãy bao gồm các sắt kẽm kim loại được bố trí theo theo máy tự phụ thuộc vào vào tài năng tham gia bội nghịch ứng chất hóa học với hóa học khác (còn call là nút độ phản ứng) của những kim loại.
Đặc trưng của dãy:
Mức độ chuyển động hóa học tập của sắt kẽm kim loại sẽ giảm dần tự trái quý phái phải
Dãy vận động hóa học của kim loại khi new học đang khiến các bạn rất khó khăn nhớ. Để rất có thể ghi nhớ nhanh dãy này, các bạn cũng có thể tham khảo mẹo dưới đây:
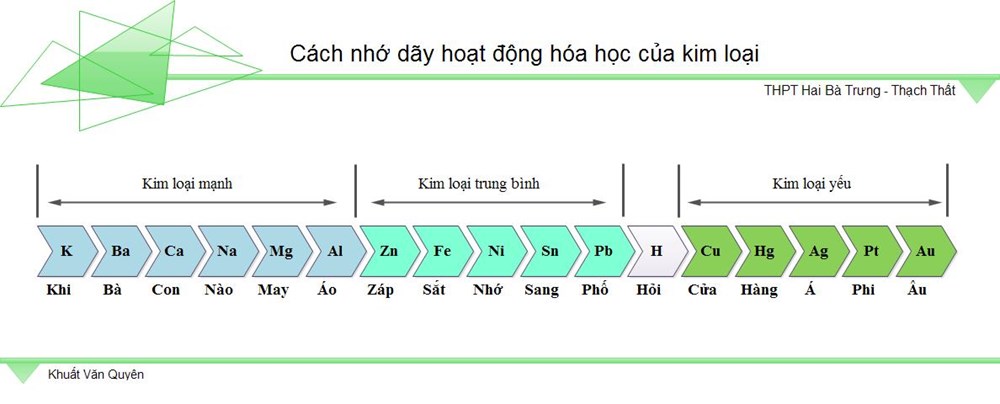
Mẹo nhớ Dãy hoạt động hóa học tập của kim loại
Hoặc Click vào liên kết sau để có thể nghiên cứu vớt dãy vận động hóa học được kĩ hơn:
https://h3qvn.com/cong-cu-hoa-hoc/day-hoat-dong-kim-loai
3. Bảng tính chảy hóa học
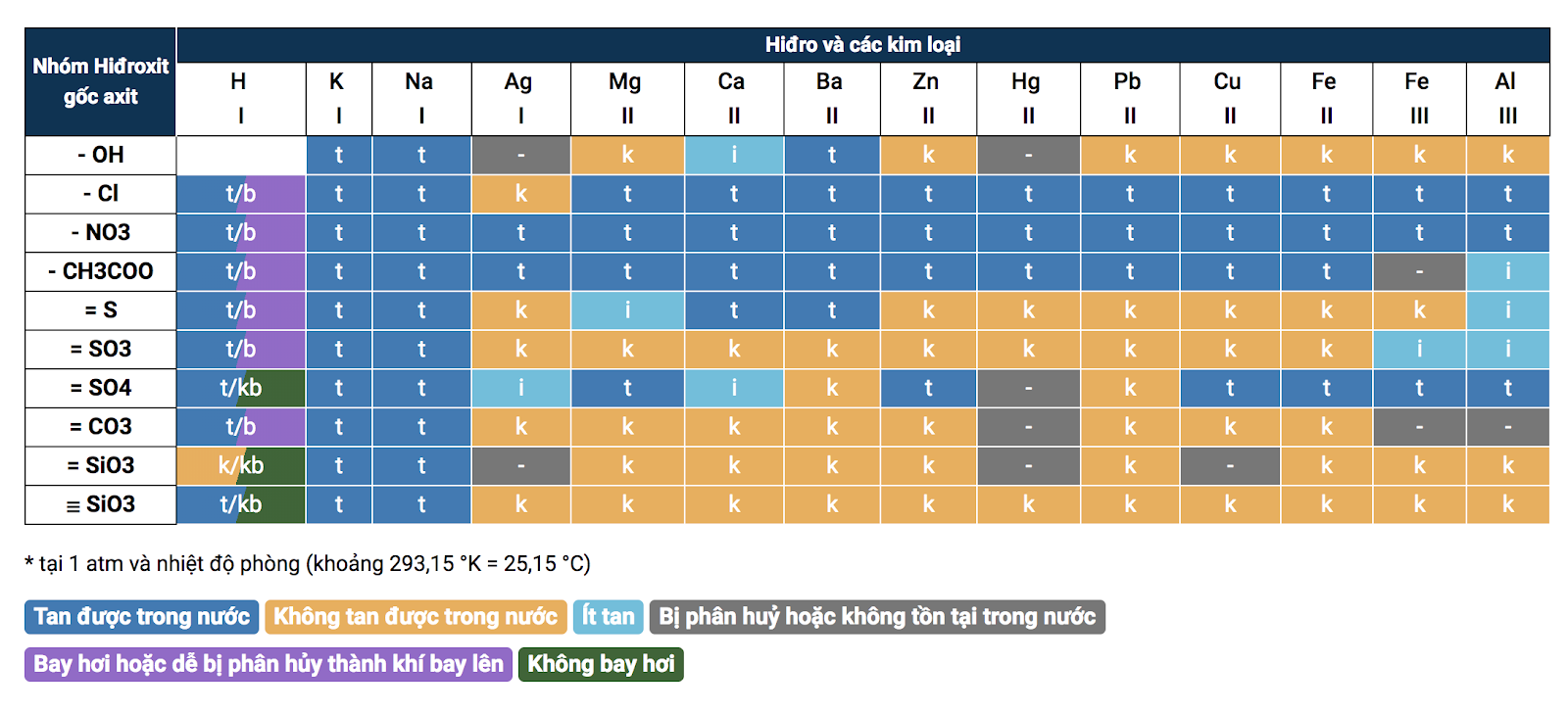
Bảng tính chảy hóa học
Bảng tính rã được dùng để làm nhận biết một chất có tan được trong nước hay không (tan nhiều, tan ít, hay không tan).
Đây là một trong công cụ có ích để các em học sinh lấy địa thế căn cứ làm những bài bác tập dạng phân biệt những chất.
Để coi Bảng tính tan cụ thể hơn, chúng ta hãy Click tại đây!
4. Dãy điện hóa của kim loại
Dãy năng lượng điện hóa của kim loại
(Xem rất đầy đủ dãy năng lượng điện hóa)
Dãy năng lượng điện hóa của kim loại sẽ đến ta biết các chất nào công dụng được với nhau phụ thuộc vào quy tắc Alpha.
Kim nhiều loại đứng trước tất cả tính khử mạnh bạo hơn sắt kẽm kim loại đứng sau
Kim một số loại đứng sau sẽ sở hữu tính oxi hóa to gan lớn mật hơn kim loại đứng trước.
III. Những chú ý trong công tác Hóa học
1. Hóa học 8
Tại Việt Nam, cỗ môn hóa học được bỏ vô chương trình giảng dạy bước đầu từ lớp 8. Các em sẽ bắt đầu được có tác dụng quen, được trình làng thế nào là chất? thế nào là nguyên tử? cố gắng nào là nguyên tố, hóa trị,.... Ở lớp này, những em học sinh phải hết sức để ý học tập, để có thể nắm rõ những kiến thức cơ bạn dạng về cỗ môn này, tránh tình trạng Mất nơi bắt đầu Hóa, gây khó khăn cho việc cải tiến và phát triển của những em ở đa số lớp tiếp theo.

Phương trình chất hóa học 8
Tổng hợp các Phương trình chất hóa học lớp 8 rất đầy đủ nhất!
2. Hóa học 9
Sau thời gian làm quen thuộc với cỗ môn Hóa lớp 8, các em cũng đã có một khối lượng kiến thức về Hóa nhất định. Sang cho chương trình lớp 9, những em sẽ tiến hành tiếp cận kiến thức và kỹ năng về các chất cơ học (bao gồm những hidrocacbon cùng dẫn xuất của hidrocacbon). Bên cạnh đó, những em đã được nâng cao kiến thức về hợp hóa học vô cơ (Oxit, axit, bazo với muối), học các khái niệm về chất new (kim loại, phi kim,...) Đây sẽ là 1 năm học với những kiến thức và kỹ năng nặng rộng năm cũ. Những em hãy cố gắng chuyên trọng điểm để không bỏ lỡ bất kì kiến thức và kỹ năng Hóa học tập 9 bổ ích nào nhé!
Xem khá đầy đủ các Phương trình hóa học lớp 9
Chi ngày tiết Giải bài tập hóa học 9
3. Hóa học 10
Tại công tác Hóa học tập 10, những em sẽ được biết kết cấu của 1 nguyên tử, chũm nào là thành phần hóa học, có tác dụng quen với bảng tuần hoàn hóa học và cơ chế sắp xếp các nguyên tố trong bảng tuần hoàn, vận tốc phản ứng, cách cân bằng phương trình hóa học,...Hãy cùng chú tâm để tiêu hóa không còn lượng kỹ năng và kiến thức khủng của chất hóa học 10 nhé!
Để giúp các em hoàn toàn có thể dễ dàng dứt chương trình chất hóa học 10, h3qvn.com sẽ sưu tầm, tổng vừa lòng lại số đông Phương trình chất hóa học lớp 10 không hề thiếu nhất, Mời các em thuộc xem trên Link: Tổng vừa lòng Phương trình hóa học 10
4. Hóa học 11
Chương trình chất hóa học 11 vẫn đưa những em tiếp cận với đông đảo kiến thức về việc điện ly, tò mò các phi kim thuộc nhóm Nito, Cacbon,... Và ban đầu được học các chất hữu cơ.

Phương trình hóa học 11
Giải bài bác Tập hóa học 11 chi tiết
5. Chất hóa học 12
Ở lớp 12, các em sẽ được học về những hợp chất hữu cơ: Este - Lipit, cacbonhidrat, amin, amino axit, polime và các vật liệu polime. Kề bên đó, những em sẽ được học các kiến thức bắt đầu về Hóa vô cơ, đôi khi ôn tập lại những kiến thức Hóa từ những lớp dưới để chuẩn bị cho kì thi tốt nghiệp trung học phổ thông cận kề. Hãy gắng gắng chuyên cần dành thời gian cho bộ môn này các em nhé!
Để rất có thể học tương tự như ôn luyện được giỏi hơn, hãy Click vào links sau: Phương trình hóa học 12 - chỗ tổng hợp các phương trình hóa học thường dùng nhất trong chương trình Lớp 12.
IV. Những công thức Hóa học phải ghi nhớ
Hóa học tập tưởng nặng nề nhưng thực chất là vô cùng dễ, nếu như khách hàng đã hiểu bản chất của những vấn đề vào Hóa học. Hãy nỗ lực thuộc nằm lòng những công thức Hóa học, để mỗi một khi cần, các bạn chỉ việc mang ra và áp dụng. Nếu làm cho được điều đó, thì Hóa đã chẳng còn là tương đối khó tí làm sao nữa. Để giúp bạn, cửa hàng chúng tôi đã đi sưu tầm với tổng hòa hợp lại được những Công thức Hóa học đặc trưng và hay sử dụng nhất. Rất ý muốn nó vẫn là cuốn sổ tay học giỏi giúp bạn vượt mặt mọi bài Hóa khó.
Click ngay để xem Tổng hợp bí quyết Hóa học tập của h3qvn.com.
Phương trình hóa học của công ty chúng tôi rất từ hào khi được cùng bạn tìm hiểu thế giới tri thức. Cảm ơn chúng ta đã thân yêu và theo dõi!












